维生素D与人类疾病的预防
维生素D是一种亲脂性类固醇衍生物,为一种激素的前体,属于脂溶性维生素,负责增加肠道对钙、镁和磷酸盐的吸收,还有其他多种生物效应。对人类而言,维生素D中最重要的化合物是维生素D2(麦角钙化醇)和维生素D3(又称为胆钙化醇)。维生素D对在钙元素的体内平衡和代谢中具有重要作用,可用以预防佝偻病和“成人骨软化症”,与钙质合用可以预防出现常见于老年人群的骨质疏松症。此外,维生素D对于神经肌肉功能、炎症都有功效,同时还影响许多基因的表达和翻译,调节细胞的增殖、分化和凋亡。
维生素D的主要天然来源是通过日光照射后在皮肤表皮的下层的化学反应生成胆钙化固醇(特别是UVB辐射),而维生素D3需由紫外线照射后,由7-脱氢胆固醇经光照进行光化学反应转变而成,动物皮肤细胞中含有7-脱氢胆固醇,因此多晒太阳是获取维生素D的简易方法。人类一天只需暴露在阳光下10分钟,自身即可合成足够的维生素D3。
两种形式的维生素D都要经过两次羟化作用,形成活性代谢物1,25-二羟基维生素D(1,25(OH)2D),当特指从维生素D3合成时,称为钙三醇(1,25(OH)2D3)。第一次羟化作用发生在肝脏,由CYP2R1编码的D-25-羟化酶将维生素D3转化为25-羟基维生素D3(钙化醇或25(OH)D3)。在DBP的帮助下,25-羟基维生素D3循环进入肾小管,由CYP27B编码的25-羟基维生素D-1 α-羟化酶进行第二次羟化,产生1,25-二羟基维生素D3(1,25(OH)2D3)。这一反应被游离钙、无机磷酸盐和最终产品(1,25(OH)2D)所抑制,而被甲状旁腺激素(PTH)所刺激,PTH是25-羟维生素D-1 α-羟化酶的调节剂。图1显示了1,25-二羟基维生素D2和1,25-二羟基维生素D3的合成途径。1,25(OH)2D负责钙的肠道运输、肾脏钙的吸收、骨骼的形成和维持、胰岛素的分泌和血压调节。为了启动这些生物过程,1,25(OH)2D与其高亲和力的维生素D受体(VDR)结合,VDR是一个配体激活的转录因子,它与视黄醇X受体(RXR)复合形成一个异源二聚体,导致维生素D反应元件识别和与这些生物过程相关的基因转录。
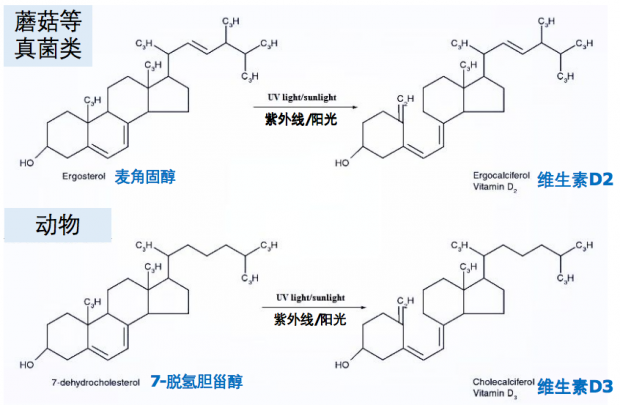
图1. 1,25-二羟基维生素D2和D3的合成
在肠道中,hetereodimer复合物的结合调节了钙结合蛋白calbindin的转录,该蛋白协助钙穿过细胞膜转移到血液中。1,25(OH)2D辅助调节calbindin的表达似乎可以控制分泌胰岛素细胞内的细胞内钙通量。1,25(OH)2D对成骨细胞的骨形成和破骨细胞的维持也至关重要。在成骨细胞中,异体二聚体诱导受体激活剂NF-κΒ配体(RANKL)的表达。RANKL与RANK受体的结合释放出一个信号级联,导致分化和破骨细胞生长。在甲状旁腺中,1,25(OH)2D参与了对PTH基因转录的抑制、VDR浓度的调节以及甲状旁腺对钙的反应。维生素D缺乏和高血压之间的相关性可能是由于1,25(OH)2D作为肾素-血管紧张素系统的负面内分泌调节剂的作用。一项实验研究表明,VDR敲除的小鼠经历了高水平的肾素表达和血管紧张素的产生,导致高血压。
除了VDR参与这些生物过程外,VDR还需要β-catenin辅助诱导成年表皮的毛囊形成。Palmer等人在用4-羟基-他莫西芬(4OHT)诱导形式的稳定β-catenin在角蛋白14启动子(K14ΔNβ- cateninER)控制下构建的转基因小鼠中证明,维生素D类似物可抑制β-catenin诱导的毛囊肿瘤形成。图2,A-C比较了维生素D类似物处理和未处理小鼠的尾部,以及野生型和K14ΔNβ-cateninER转基因小鼠的染色尾部切片。Palmer等人,也报道了在没有VDR的情况下,β-catenin会诱发人类肿瘤,其特征是浸润性基底细胞癌。图2,D和E显示了用β-catenin和VDR标记的trichofoluloma和基底细胞癌的人类皮肤切片。实验研究认为,VDR是Wnt途径的转录效应器,促进毛囊分化并调节Wnt诱导的肿瘤形成。这项调查是最近研究的一个例子,使人们更深入地了解维生素D参与癌症相关机制。

图2. VDR调控β-catenin诱导的皮肤肿瘤
研究表明,维生素D的缺乏与结肠癌、前列腺癌、乳腺癌、卵巢癌、淋巴瘤和其他破坏性的癌症类型有关。据称,将人口的平均循环25(OH)D水平提高到约50ng/mL,每年可预防约58,000例乳腺癌和约49,000例结肠直肠癌。然而,由于有效的治疗水平可能会产生高钙血症,所以上限的剂量限制是至关重要的。这些信息是基于观察性研究与随机试验相结合的结果。预防癌症的维生素D指南侧重于25(OH)D的水平,而不是血液中的1,25(OH)2D,因为1,25(OH)2D的产生是由肾脏严格控制的。
通过阳光照射或饮食摄入增强的维生素D水平不会导致1,25(OH)2D产生的可测量的增加,但确实会导致25(OH)D浓度的可测量的增加。肾脏不是25(OH)D羟化的唯一位置;多种组织,包括皮肤、乳房、结肠、肺和大脑都有将25(OH)D代谢为1,25(OH)2D的能力。有人认为,提高血液中的25(OH)D水平可提供足够的25(OH)D底物,使各种组织类型能够利用本地合成的1,25(OH)2D来保护细胞不受控制地生长和成熟以及恶性肿瘤风险。
细胞生长和成熟控制可能归因于维生素D的抗血管生成特性。Mantell等人显示,对 "激活的 "内皮细胞进行1,25(OH)2D处理可明显抑制血管内皮生长因子(VEGF)诱导的内皮细胞萌发和延伸,这是血管生成过程的一个必要阶段。另一项体内研究显示,1,25(OH)2D处理产生的肿瘤比没有1,25(OH)2D处理的小鼠形成的肿瘤的血管化程度低。
以前关于维生素D和癌症的研究结果导致了一个新的癌症病因学模型的产生,被称为DINOMIT(分离、启动、自然选择、过度生长、转移、内卷和过渡)。该模型描述了细胞之间的交流丧失是癌症发展的驱动力。这个新模型与致癌性和癌症干细胞模型有很大的不同。加州大学旧金山分校的塞德里克-加兰说:"在这个新模型中,我们提出这种损失可能在癌症中发挥关键作用,因为它破坏了对健康细胞周转至关重要的细胞之间的沟通,使更具侵略性的癌细胞得以接管。" 当有足够的维生素D水平时,细胞会粘附、交流,并作为成熟的上皮细胞行事,但如果维生素水平不足,它们可能会失去粘性,同时失去作为分化细胞的身份,并恢复到干细胞的状态。加兰进一步指出,"维生素D可能通过重建具有完整维生素D受体的恶性肿瘤的细胞间连接来阻止癌症过程的第一阶段"。
尽管DINOMIT模型和本文介绍的其他科学报告为维生素D的有益价值提供了有力的解释,但还需要更多的研究和长期的临床研究来充分了解维生素D对人类疾病预防的影响。